AiSci:論生物製藥模態的商品化
原文作者:Elliot Hershberg
編譯:LlamaC
正文?
十年前,科學論派信徒(不是科學家)鮑勃·杜根將他創立的美國生物技術新創公司以210 億美元(沒錯,不是百萬)的價格賣給了艾伯維。他的公司Pharmacyclics 研發出一款極具前景的抗癌藥物,並因此獲得了豐厚回報。實際上,據報道,杜根超過35 億美元的收益是歷史上公開收購案例中回報最為豐厚的之一。
除了創始人杜根的特立獨行——以及其他幾位大人物參與其中,使整個事件足以載入史冊——這原本是一筆相對普通的交易。一家大型製藥公司因其一款重磅產品的專利獨佔期即將結束,正面臨尋找新收入來源的巨大壓力。而一家美國新創公司的突破性藥物恰好填補了這一空缺。
生物技術產業的很大一部分正是建立在這種動態之上。小型新創公司已成為創新的主要來源,每年承擔大部分早期臨床試驗。大型製藥公司則以豐厚溢價收購這些新創企業,並持續補充其產品管線。
但情況正在改變。十年後,杜根捲土重來。這次,他帶來了在臨床試驗中擊敗默克公司年收入300 億美元的癌症免疫療法藥物Keytruda 的新藥。關鍵在於,杜根並非在美國實驗室發現此藥,而是從一家中國公司獲得了授權。
與Pharmacyclics 不同,這個故事並未以數十億美元的天價收購告終。相反,默克公司轉向同一來源,以5 億美元從另一家中國公司購得了同類型藥物的自有版本。
這意義重大。正如我們最近在人工智慧領域所見,中國已成為生物科技領域不可小覷的競爭威脅,展現出快速開發能與美國實驗室產品匹敵——甚至超越——的新藥能力。換言之,“製藥業正迎來其' deepseek 時刻'。”
再舉一個例子。隨著GLP-1 類藥物爆炸性成功,製藥公司競相獲取自己下一代此類產品,以與諾和諾德和禮來爭奪市場份額。默克再次將目光投向中國,以1.12 億美元預付款收購了一款口服GLP-1 藥物。該交易還包含基於商業成功的後續里程碑付款,總額達19 億美元。
作為背景,美國生物製藥公司Viking Therapeutics 在其研發管線中擁有一款口服GLP-1/GIP 激動劑,目前市值38 億美元。與其全面收購Viking,為何不從中國低價取得一個分子,看看它是否有效?
在生物技術市場低迷的時刻,加劇的外部競爭使情況更加艱難。雖然併購市場已經放緩,但現在創辦人和投資者都因為那些他們從未聽說過的隱密中國競爭對手在最後一刻攪黃交易而夜不能寐。
整個局勢引發了大量分析。到目前為止,我最欣賞的有美籍華人生物科技新創公司創始人David Li 的反思、他在Timmerman Report 中的後續分析、彭博社的報道,以及Alex Telford 對「我們所有的藥物都會來自中國嗎?」這一問題深思熟慮的見解。
在這裡,我想退一步思考我們是如何走到這一步的。
1987 年,默克公司因"押注神奇分子"登上《財富》雜誌封面,被評為"美國最受尊敬企業"。

在此之前幾十年,默克公司的科學家負責研發了針對高血壓的突破性分子、歷史上一些最成功的疫苗(史上最多產的疫苗學家之一莫里斯·希勒曼曾是默克的科學家)、首批他汀類藥物以及全新類別的抗生素。
如今,對於市場上最熱門的兩款產品,默克公司並未依賴美國生物技術新創企業生態系統(該體系在1987 年仍處於艱難起步階段),而是從中國生態系統中獲取分子——直到最近,中國才成為創新的重要來源。
顯然,全球藥物研發產業已經經歷了顯著的演變。在此關頭,我認為有必要思考藥物研發技術商品化的漫長歷程,以及這段歷史模式對產業未來的影響。
藥物研發技術商品化的漫長歷程
讓我們來思考一下生物製劑。
在歷史長河中,絕大多數藥物都是人類偶然發現的、對人體生理有正面影響的植物性化學物質。隨著時間推移,人們開發出工具,能更有系統地篩選化學空間以尋找有用的小分子。另一小類則是諸如胰島素等可從動物體內分離並用於治療疾病的蛋白質。
1976 年基因泰克的成立源自於重組DNA 技術的革命性突破,這項變革播下了徹底改變的種子。透過基因工程工具,人們得以以全新方式生產生物源性分子來緩解疾病。五十年後,每年核准的生物製劑數量已幾乎與小分子藥物持平。
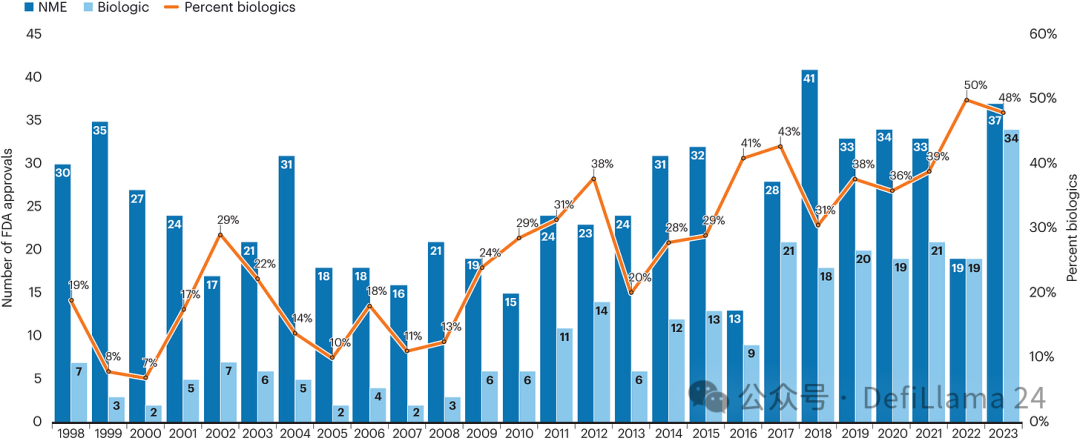 生物製劑隨時間的成長
生物製劑隨時間的成長
但最初,很少人相信這種新型藥物會成為可能。而且,全世界具備嘗試所需必要技能的人也同樣寥寥無幾。人們很容易忽略一個事實:基因泰克最初只是一個邊緣項目,科學家們日夜工作,穿著統一的T 卹、牛仔褲和跑鞋。
正如彼得·蒂爾所言,這家公司掌握著一個重要的共同秘密,而外界尚未理解。
成功改變了這一切。當基因泰克取得首個產品突破時,市場以狂熱的樂觀態度回應。沒有什麼——甚至戴安娜王妃——比改造生命更令人興奮。

1980 年基因泰克上市時,初始股價為35 美元。交易開始僅一小時,股價便飆升至88 美元,幾乎翻了三倍。當時的場面簡直是一片狂熱。
到1983 年,美國公司已向新興生技企業投資了5 億美元。兩年後,美國商務部估計約有200 家生技公司總共吸引了近20 億美元的投資。
回首往事,這顯然是一個炒作泡沫。重組DNA 技術當時仍處於起步階段。像重組胰島素這樣的重大突破並未迅速接踵而至。監管問題依然懸而未決。大規模生產生物製劑也是一項挑戰。
最初的繁榮過後是一段幻滅與收縮的時期。 1985 年,馬薩諸塞州的一位記者寫道:
如果這一切對幾乎沒有或完全沒有商業記錄的科學家來說顯得太遠,那麼你是對的。僅此一點,在後繁榮時代的生物技術產業中,兩種趨勢已佔據主導地位。
首先,在少數資本較為雄厚的公司中,科學家/創辦人/執行長們正在聘用,或被迫聘用傳統的「數位專家」擔任公司總裁或營運長。這些是來自大公司的經驗豐富的商業主管,而非學術界的學者。位於劍橋的BioTechnica International 剛剛聘請了一位在杜邦公司工作20 年的資深人士。在鄰近列剋星敦的Collaborative Research,新任總裁曾領導強生的一家子公司。位於尼德姆高地的Damon Biotech 的新總裁也是如此。
其次,產業動能似乎已轉向有利於大公司。尤其是那些透過股權購買和研發合約為生物技術新創公司提供大量原始資金的公司。從某種意義上說,新生技公司首次公開募股的良好反應,只是推遲了許多公司的壞消息。如今,當這些年輕公司急需新一輪資金注入時,杜邦、格雷斯公司、孟山都和禮來等公司卻將投資轉向內部生技能力。因此,產業專家預測將出現一波併購潮。 EF Hutton 分析師尼爾森·施耐德認為,多達三分之二的生技公司要么合併,要么被大型製藥或化學製造商收購。
換句話說,該行業被迫走向成熟並真正實現收入,現有組織也醒悟過來,開始內部建構自身的生物技術能力。到了1980 年代末,大多數生技股票已損失四分之三的價值。
但在這泡沫的核心,有一個重要的真理內核:重組DNA 技術確實是製造新藥物的革命性工具。即便在較冷靜的環境中,那些擁有資源、技術、人才和毅力得以生存的公司,仍不斷推出新產品。
在合成胰島素之後,基因泰克在整個80 年代和90 年代又生產了七種生物製劑。安進公司是另一家成立於1980 年的早期生物製劑先驅,他們憑藉一系列突破性藥物在激烈的競爭中脫穎而出。再生元公司成立於1988 年,在最初的繁榮之後,他們透過對人類基因組的深入研究及強大的單株抗體生產技術平台逐漸確立了自身特色——單株抗體被證明是最重要的生物製劑類型之一。
儘管仍有許多懷疑者,生物製品的應用範圍仍在醫學領域持續擴大,到2022 年其核准數量首次與小分子藥物持平。 (我們之前看到的圖表。)
這些先行者的商業成功同樣不可否認。基因泰克於2009 年被羅氏以468 億美元收購,至今仍以極具影響力的獨立子公司運作。安進目前市值達1,680 億美元。再生元現估值780 億美元,股價較首次公開募股時上漲近4,000%。 2
這個演變過程幾乎是Gartner 炒作週期的教科書式範例。最初的"創新觸發點"引發了一輪巨大的炒作和興奮浪潮。當炒作未能立即兌現時,市場便趨於冷靜。若初始觸發點確有實質內容,則隨著時間的推移會出現更為漸進式的回升。
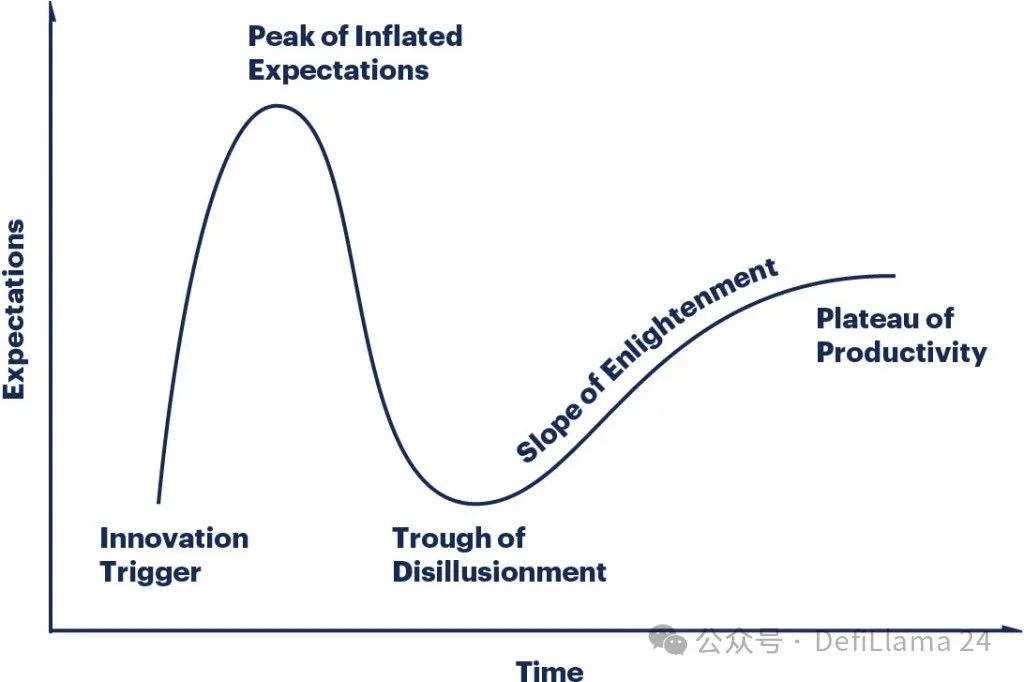
我們似乎確實已經進入了一個「生產力高原」。生產生物製劑的能力不再是少數公司嚴守的秘密。全球科學家已經花費數十年時間完善開發這些藥物的工具。一大批公司如雨後春筍般湧現,提供抗體開發服務。
以Adimab 為例。該公司成立於2007 年,利用新一代抗體工程技術——即酵母表面展示技術——為許多合作夥伴快速生產新分子。目前,他們已與超過一百家不同夥伴合作,「源自我們平台的臨床計畫超過75 個」。
 源:Adimab
源:Adimab
鑑於Adimab 是一家私人公司,很難將其商業成功與安進或再生元等先行者進行直接比較。但從十年前一筆二級交易中11 億美元的估值推算,大致已成長為約5,000 至100 億美元規模的企業。
如今,若企業希望採用不同技術,或在成本、速度、地理位置甚至其他多種因素上有特定偏好,他們可以選擇與FairJourney Biologics(2024 年估值約9 億美元)、OmniAb(市值約4 億美元)、Ablexis、Specifica、Creative Biolabs、Twist Biosciences、Alloy Therapeutics 或其他公司合作。此清單僅為範例,遠未窮盡所有選項。
值得注意的是,每一代企業的規模大約下降一個數量級。先行者成長為約1,000 億美元以上的公司,隨後崛起的領先服務供應商成為約100 億美元以上的企業,而如今發現市場的新進業者則是約10 億美元以上的公司。
在我看來,這就像是教科書上對商品化的定義,即逐步將商品或服務轉化為大宗商品並在價格上展開競爭的過程。大宗商品指的是可以與其他同類商品互換的商品或服務。
想想電子產品。最初,只有少數幾家公司能生產出最好的電視,這些公司因此收取高額溢價。隨著時間的推移,這種溢價被競爭消磨殆盡。如今,眾多公司在好市多以數百美元的價格銷售配備智慧功能的大尺寸平板螢幕。這就是商品化的過程。
同樣,抗體發現服務提供者之間的差異越來越難以區分,許多公司使用相似的技術針對相同的藥物標靶生產抗體。
到目前為止,我們只關注了抗體的歷史。但我想請你和我一起大膽假設,這可能會惹惱一些藥物開發者:沒有任何發現技術能免受商品化這一不可避免趨勢的影響——就像幾乎所有其他技術一樣。
對於大小分子而言,一旦發現技術——無論是高通量篩選、電腦模擬篩選、體外或體內模型,還是分析檢測——實現標準化,全球各地的公司將競相將其作為服務提供。
這是模態商品化的漫長歷程。
隨著時間的推移,革命性的概念成為下一波創新的普遍基石。
生物技術的戰略演進
在發現技術標準化和商品化的同時,生技投資也走向專業化。經過數十年的精進,該行業趨向於採用標準化的公司估值模型,並湧現新的策略。
一種已獲得廣泛認可的策略是“快速跟隨者”方法,即開發一種新藥,使其在已有藥物針對的靶點上成為“同類最佳”,而非針對全新藥物靶點成為“首創”。
2003 年發表的一項分析指出了「追求最佳」的兩大關鍵優勢。首先,這類藥物顯然具有更低的風險特徵,因為其標靶已通過基於人體證據的藥物審批得到驗證。投資人通常會討論他們為新標靶假設所承擔的「生物學風險」程度。其次,風險差異似乎並未獲得相對應的報酬。事實上,觀察1991 年至2000 年間推出的藥物,大多數重磅炸彈藥物都是針對已知標靶開發的,而快速跟進者創造的價值高於風險更高的創新藥物。
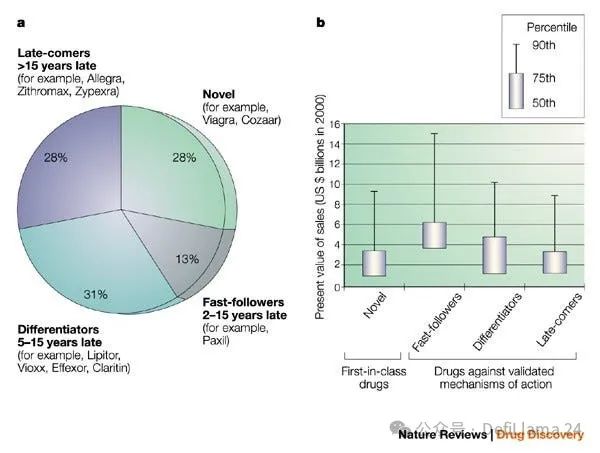 追求最佳
追求最佳
默克公司收購我們先前研究過的口服GLP-1 激動劑,就是這項策略的鮮明例子。諾和諾德與禮來公司在驗證首批GLP-1 藥物療效時承擔了巨大風險。如今,其他公司正競相開發具有改良特性的快速跟進產品,例如以藥丸形式取代注射給藥。
許多生物科技投資者已將此類分析推向了邏輯的極致。隨著早期融資輪次規模及其背後資金的膨脹,將大量資本押注於完全未經證實的標靶假說上愈發難以自圓其說。實務中,這導致已驗證標靶領域出現了嚴重的紮堆現象。
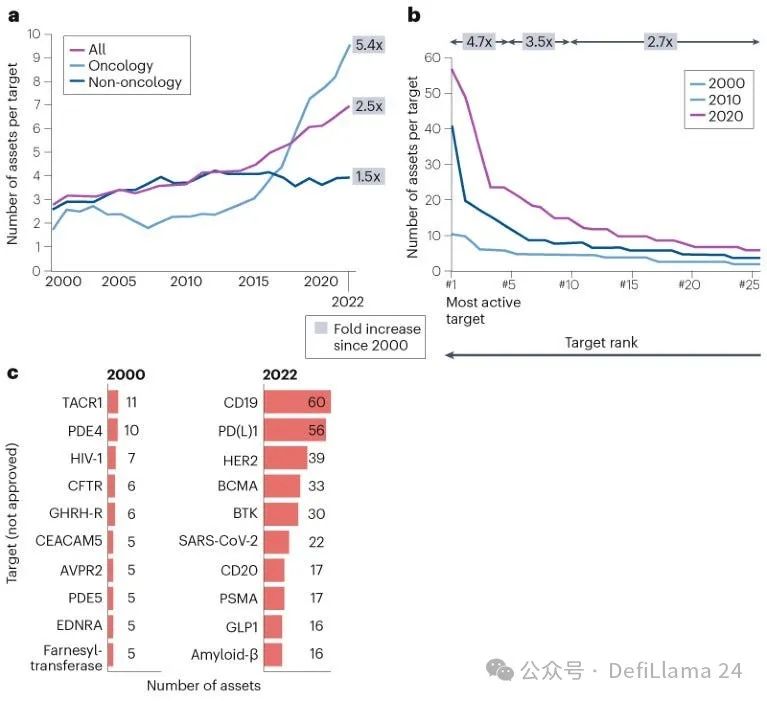 藥物研發管線中的聚集現象
藥物研發管線中的聚集現象
為了讓事情更加高效,2010 年代左右興起了“虛擬生物技術公司”,它們將所有研發工作外包給像Adimab 這樣的發現合作夥伴。其目標通常是快速開發出針對已知標靶的最佳分子,然後將其出售給大型製藥公司進行後期開發和商業化。
這段行業歷史對於理解近期中國許可協議的激增至關重要,因為許多頂級外包合作夥伴都是中國的合約研究組織(CROs)。
藥明生物,這家提供全方位生物製劑發現與製造服務的中國巨頭企業,已躍居全球第二大外包合作夥伴,佔據了超過10%的全球市場份額。
如今,中國在2015 年新政策中體現的極具邏輯性的策略演變,是從單純的服務提供者轉向自主研發藥物。在多數人使用標準化發現技術針對相同藥物標靶的世界裡,中國有兩大關鍵優勢:
速度。新的一系列改革使得臨床試驗能夠更快地啟動。
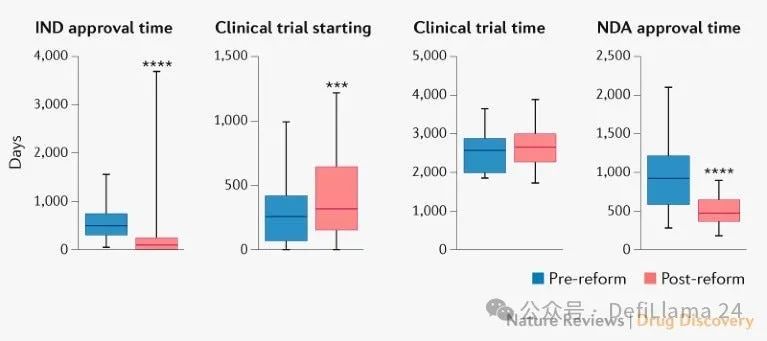 中國創新藥物研發趨勢(再次感謝Alex Telford 的精彩部落格文章讓我注意到這一數據!)
中國創新藥物研發趨勢(再次感謝Alex Telford 的精彩部落格文章讓我注意到這一數據!)
成本。中國科學家的薪資僅為美國科學家的一小部分。一支由高技能——通常受過美國訓練——研究人員組成的大軍可以投入更多問題的研究。
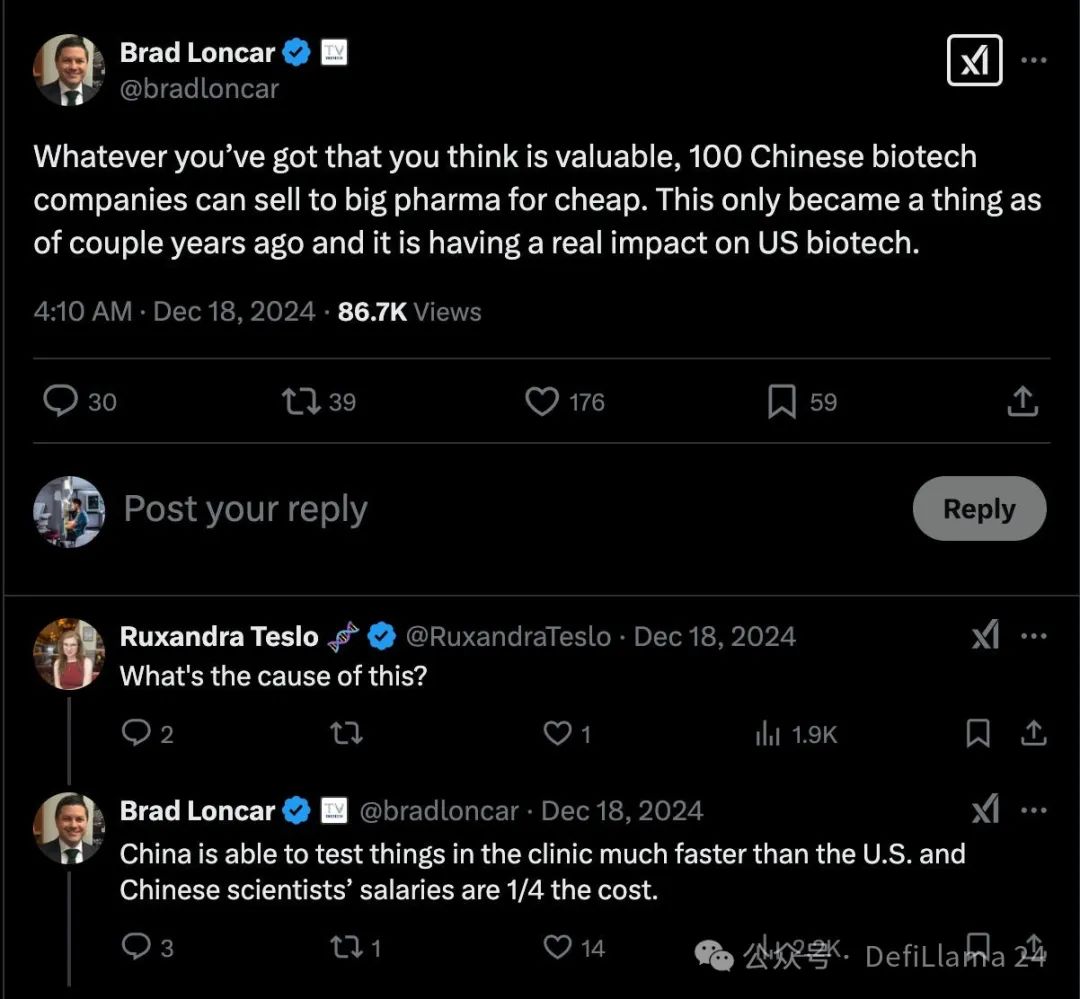
憑藉這些優勢,中國的新創公司和生物製藥公司似乎已經涵蓋了已知藥物標靶的領域。企業以臨床前或早期資產的形式,對廣泛靶點佈局廉價的「買權」。當某一特定標靶或產品構想獲得大型製藥公司青睞時,這些「選擇權」便可透過加大投入加速現有專案進程來執行。
這給快速跟隨策略帶來了巨大壓力。當美國科學家在夜晚入睡時,地球另一端競爭對手實驗室裡的機器仍在嗡嗡作響。
到目前為止,我們已經追溯了藥物發現技術商品化的歷史以及隨之而來的生物科技投資專業化。這些變化有助於為行業的「DeepSeek 時刻」提供背景。
現在,讓我們思考未來價值可能累積的領域。
人工智慧可能是最後一波商品化浪潮
過去幾年,大量資金湧入那些懷抱雄心壯志、旨在利用人工智慧變革藥物研發的公司。像Xaira Therapeutics 這樣以10 億美元「種子」資金起步的企業,目標是自主研發藥物。但EvolutionaryScale、Profluent、Chai Discovery 和Latent Labs 等許多公司則更傾向於採取類似Adimab 的策略,將這項新技術作為廣泛賦能的基礎設施來提供。
當Latent Labs 成立時,Pillar 的Tony Kulesa 寫道:
由此誕生了一個清晰的願景:在藥物發現領域普及先進人工智慧工具的使用。儘管每家尋找治療分子的生物技術和製藥公司都明白人工智慧的作用,但大多數公司並不具備開發自己前沿模型和工具的能力。西蒙的洞見在於,透過讓合作夥伴即時獲得最佳工具,Latent Labs 能夠加速整個產業的藥物設計進程。
大規模融資與新商業模式的結合引發了好奇又懷疑的複雜反應。 Endpoints 的Andy Dunn 寫道:「Latent 的成立展示了以AI 為核心的新創公司如何能在生物科技領域打破傳統。大多數生物科技公司圍繞某個分子、研究論文或關鍵知識產權成立,而Latent 的投資者則押注於Kohl 和另一位前DeepMind 開發者、AlphaFold 的投資者則押注於Kohl 和另一位前DeepMind 開發者、AlphaFold 的客戶 Alex Briland 的出路才能找到出路。
讓我們考慮這項投資論點的熊市情況和牛市情況。
在熊市情況下,與商品化技術相比,無論是專注於新資料產生、模型擴展、架構改進,或是這三者的某種組合,這些技術方向都無法顯著推動進展。
在麻省理工學院分子機器學習會議的現場筆記中,Dimension 的西蒙·巴尼特寫道:“我對[Adimab 聯合創始人]威特魯普博士演講的理解是,他認為單克隆抗體(mAb)發現基本上是一個已解決的問題,而機器學習(ML)對這一領域的影響被誇大了。”
如果人工智慧技術最終僅對抗體發現等問題產生微小的量化影響,提供這些解決方案的公司可能會加入眾多競爭提供此類服務的公司行列。我們可能會看到市值低於10 億美元的公司,而非約500 億至1,000 億美元以上的世代巨頭。
牛市的情況如何?跟我一起瞇起眼睛想像一下,AI 的進步軌跡將帶來質的飛躍,真正引領我們進入一個設計而非發現的世界。想像一個模型,它能零樣本預測柏拉圖式抗體-對任何標靶都具有完美的親和力和特異性,在每個維度上都經過極致優化。輸入目標產品特性(TPP),就能得到一種藥物。
那可能會是件大事。
一個常被引用的比較對像是Cadence Design Systems,這家市值660 億美元的公司大部分收入來自向半導體產業授權其電子設計自動化(EDA)軟體和智慧財產權。在高價值領域,最佳設計工具可能極具價值。那麼,「製藥業的Cadence」是否會規模更大?
有證據支持這項技術發展軌跡嗎?
去年三月,華盛頓大學的貝克實驗室發表了一篇題為《原子精度從頭設計單域抗體》的預印本論文。基於數十年來在計算蛋白質設計領域的領先工作,他們引入了一個AI 模型,能夠有效為特定標靶生成微型抗體(稱為VHHs 或奈米抗體)。
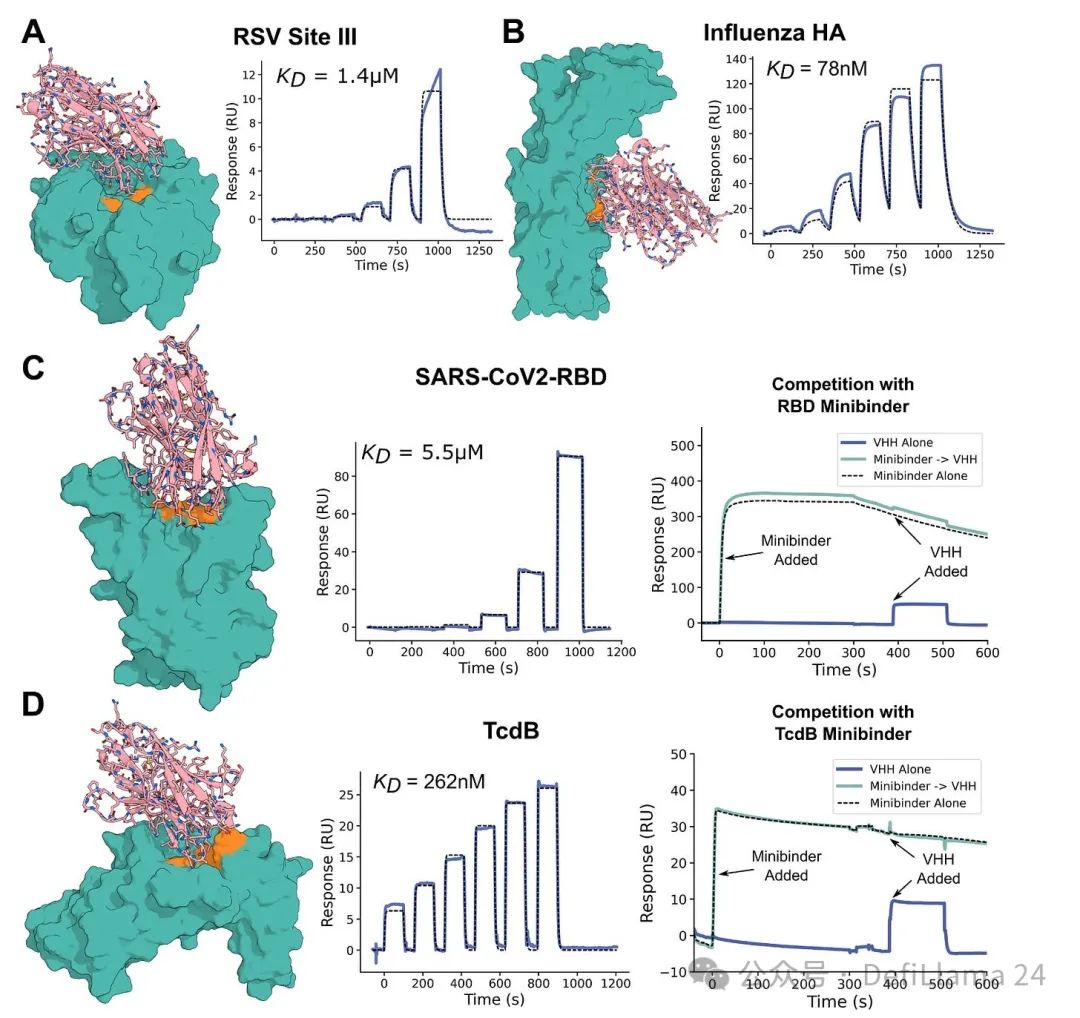 圖2 部分內容:原子精度從頭設計單域抗體。結合劑以粉紅色顯示,目標蛋白為青綠色。指定的抗原決定基(即抗體結合的區域)以橘色顯示。
圖2 部分內容:原子精度從頭設計單域抗體。結合劑以粉紅色顯示,目標蛋白為青綠色。指定的抗原決定基(即抗體結合的區域)以橘色顯示。
這些結果激起了巨大的興奮和興趣——包括為啟動Xaira 投入的10 億美元賭注。但這項工作只是概念驗證,而非能吐出完美抗體的神奇黑盒子。科學家指出,所生成的奈米抗體對其標靶的親和力仍然太弱,無法成為藥物。而且奈米抗體是一種奇怪的蛋白質,與人類抗體並不完全相似——這再次限制了它們在許多臨床應用中的效用。
不到一年後,Baker 實驗室「顯著更新」了他們最初的預印本,將其更名為《使用RFdiffusion 進行原子級精確的抗體從頭設計》。 正如你可能猜到的,標題之所以更改,是因為研究範圍已擴展至VHH 設計之外。更新後的預印本也展示了單鏈可變片段(scFvs)的設計,這是另一種抗體形式,擁有兩個可變域,而非VHH 的單一可變域。
另一個重要更新是針對親和力問題的回應。作者寫道:「雖然初始計算設計顯示的親和力一般,但利用OrthoRep 進行親和力成熟可以生產出保持預定表位選擇性的個位數納摩爾級結合物。」換言之,人工智慧目前尚不能產生完美的結合物,但可以透過現有實驗技術快速調整優化。
所以這大約是一年的時間。冒著在兩個數據點之間劃線的風險,進展似乎相當迅速。展望未來,如果有人利用OrthoRep 創建了一個龐大的親和力訓練資料集,而這一步脫離了原子的領域,以改進模型權重的形式編碼在比特的世界中,那會怎麼樣?
未來五年,是什麼會阻礙從VHHs 到scFvs 再到成熟單株抗體的持續發展?
再次粗略觀察,我們似乎正處於生物製劑開發數位化的邊緣。如果速度、成本——可能還有品質——方面的優勢足夠顯著,這可能導致發現市場的整合,新進入者迅速吸引大量外包工作份額,取代現有企業。
現在讓我們認真思考一下「基礎模型」這個概念下的世界會是什麼樣子。如果生物結構和功能的重要基礎模式是透過眾多任務學習而來的呢?正如Latent Labs 的Simon Kohl 對Endpoints 所說:“這一願景更為宏大。我認為我們可以在此基礎上擴展,隨著時間的推移,我們會發現分子相互作用層面之外的許多其他領域也能通過生成模型來引導。”
因此,如果這一點——或我剛才概述的任何部分——屬實,其中一些公司可能會變得非常龐大。
但最大的威脅之一很可能是…商品化!畢竟,整個「deepseek時刻」的框架源自於中國研究團隊在資源少於美國同行的情況下,AI 能力突然實現飛躍。
已有跡象顯示這一點。
迄今為止,諾貝爾蛋白質結構預測獎的共同獲獎者、DeepMind 和Isomorphic Labs 的執行長德米斯·哈薩克斯一直押注於演算法創新,而非建構專有數據護城河來確保模型防禦性。在最近的一次採訪中,他表示:“讓你的演算法更好,讓你的模型更優。你確實擁有足夠的數據——只要你在演算法方面足夠創新。”
令人驚訝的是,嚴肅的演算法競爭者如此迅速地湧現。
2024 年5 月,Isomorphic 與DeepMind 發表論文,介紹了其最新且最先進的結構預測模型AlphaFold3。同年9 月,Chai Discovery 發布並開源了一款尖端模型。約兩個月後,麻省理工學院的研究團隊又推出了相當效能的另一個開源版本。
在這場新的人工智慧競賽中,價值將如何累積值得關注。
無論如何,所有這些進展都將為藥物研發和其他環節的創新開闢新機會。
發現平台可能變得更有價值
並非所有生物技術平台都專注於治療模式。一些公司關注的是硬幣的另一面:識別新的生物標靶以開發藥物。在史蒂夫·霍爾茨曼的「平台公司類型學」中,這些被稱為「洞察平台」。
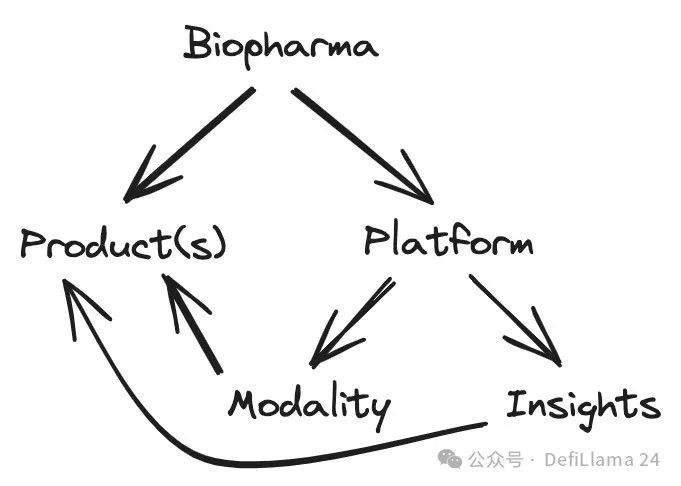 關於生物技術平台策略
關於生物技術平台策略
專注於疾病洞察也伴隨著一系列策略挑戰。 Holtzman 在其原始帖子中寫道:
然而,2 類A 型平台公司面臨一系列1 類平台公司未曾遇到的挑戰。這些挑戰本質上源自於2 類A 型平台公司的產出是數據/資訊/洞察,而非如1 類平台公司生產新化學實體(NCEs)和生物治療藥物。
- 生物製藥產業的數據歷史就是其商品化的歷史。
- 以藥品/產品為"生命線"的公司有著既得利益,將數據"預先競爭化"(或至少在獨佔一段時間後這樣做)。他們憑藉產品取勝;不願被資訊擁有者束縛。
- 智慧財產權(IP)環境日趨嚴格:過去僅憑展示某基因在病變組織中過度表達(或疾病狀態下的基因突變)的轉錄譜,就能獲得「透過任何方式調節靶點A 以治療疾病X 的方法」這類邏輯形式的專利授權(附帶權利要求說明「方式」可以是抗體、反義核酸、RNA 幹擾、基因形式的專利授權(附帶權利要求說明「方式」可以是抗體、反義核酸、RNA 幹擾、基因治療、返小分子等)的日子已被返復不復和基因治療、返不復合等)。
- 此外,隨著時間的推移,客戶群的需求變得更加廣泛。在1990 年代,大多數大型製藥公司的客戶願意接受將數據使用限制在小分子藥物發現和開發上的條款(因為這是他們唯一從事的領域),而如今,所有製藥公司/大型生物技術公司都會要求獲得利用這些數據進行所有治療模式開發的權利。
- 最後,Genus 2, Species A 平台公司在資料的產生、管理和分析方面擁有並建構了其專業知識。它並不具備或無法承擔在一個或多個治療模式中藥物發現/開發的重大能力投資,或在一個或多個疾病領域的深入生物學/轉化能力培養。
- 最終結果:Genus 2, Species A 平台公司放棄其數據/資訊業務,轉而建立並成為藥物發現與開發企業。
讓我們分解一下。
首先,重要的是要認識到資料生成技術本身也經歷了一個漫長的商品化過程。 (這就是技術,各位!)其次,過去的主要問題在於與大型合作夥伴的不對稱談判——他們曾獨佔發現技術,這使他們在針對新靶點實際創造化學物質時擁有不公平的優勢。
這種動態已經開始轉變。 CRO 產業的成長和成熟已經使得洞察公司能夠帶著自己的新化學實體(NCEs)而非僅僅是圍繞目標洞察的專利參與合作夥伴討論。
如果人工智慧加速了這項動態會怎麼樣?隨著時間的推移,隨著模式變得越來越商品化,從目標洞察到可開發化學物質的時間和成本可能會進一步壓縮。
在這個世界秩序中,天平可能會發生傾斜。針對已知標靶的新疾病見解,其價值可能超越化學空間中任何漸進的起點。
畢竟,GLP-1 藥物超過1000 億美元的成功故事建立在生物學洞見之上,而非技術模式的進步。
有幾個經濟和技術現實可能會減緩這方面的進展。
在經濟層面,正如David Yang 精闢指出的那樣,GLP-1 之所以成為製藥業的成功案例而非生物科技公司的勝利,部分原因在於併購在該行業的核心地位。大多數早期生技投資者都寄望於透過大型收購實現資金流動,這意味著他們密切關注製藥巨頭的收購清單。而製藥買家確實不願斥資數十億美元去驗證新的生物學假設——尤其是在市場機會規模尚不明朗的情況下。
我們如何改變這一現狀,釋放出更具創新性藥物的新浪潮?我們需要繼續縮短從發現、開發到商業化的每個環節的時間和成本。
這樣做將使早期藥物發現變得更有價值。
提升發現和商業化能力看似都是技術問題。加速發展可能需要新技術和監管改革。借鏡中國的經驗(這次換一換思路!)並研究其近期的改革舉措,或許能為後者提供一個好的起點。
在技術層面上,重要的是要認識到,模擬人類生物學比模擬特定模式是一個更困難的AI 問題。考慮兩個問題:我的抗體是否以更高的親和力結合這個標靶?活化GLP-1 受體會對整個人體生理產生什麼影響?實驗室中明確回答第一個問題的工具已經具備。而第二個問題的答案只有在首次人體試驗後才能完全知曉,因為我們的臨床前模型只是人類生物學的粗略近似。
更有效地模擬人類生物學可能需要大量數據生成和在新人工智慧範式上的持續進展。
隨著時間的推移,應對這些經濟和技術挑戰可能會極大重塑生物製藥行業的格局,引領一波新興商業生物技術公司推進大膽新療法的浪潮。
但從長遠來看,所有這些快速疊加的技術也可能導致與傳統生物技術商業模式更徹底的背離。
護城河可能大不相同
在大多數行業中,存在多種可行策略以建立持久的競爭優勢。 Hamilton Helmer 提出的經典7 Powers 架構旨在列舉最普遍採用的方法。
7 大力量分別是:
- 規模經濟-隨著產量增加,單位成本下降的企業。
- 網路經濟-一種隨著使用者基礎擴大,客戶實現的價值也隨之增加的商業模式。
- 逆向定位-企業採用一種新的、更優越的商業模式,而現有企業由於擔心現有業務被蠶食而無法效法。
- 轉換成本- 一種商業模式,顧客預期因轉向替代方案而遭受的損失大於所獲得的價值。
- 品牌效應-由於歷史資訊的影響,一個企業在提供客觀上相同的產品或服務時,享有更高的感知價值。
- 受困資源-一家企業擁有某種令人垂涎的資源的優先取得權,而這種資源能獨立提升價值。
- 流程力量-一個企業的組織結構和活動組合能夠實現更低的成本和/或更優質的產品,這些優勢只有透過長期投入才能匹敵。
冒著過度簡化的風險,在生物製藥領域,只有兩種力量真正重要。大型製藥公司受益於規模經濟,因為它們能夠透過現有產品組合的收入分攤開發和商業化的成本。而對於生技公司來說,基本上唯一真正的力量來源是以新智慧財產權(IP)形式控制的壟斷資源。
正如彼得‧杜拉克曾寫道:「製藥業是資訊產業。」小分子藥物的價值與其物理形態無關,後者幾乎不值錢。能夠對任何現有實體產品收取最高利潤,純粹是智慧財產權的功能。一旦智慧財產權到期,仿製藥製造商就能迅速介入,提供大幅降低的價格。
這就是RA Capital 的彼得·科爾欽斯基所定義的「生物技術社會契約」。科學家和企業家因創新而獲得專利獨佔權的獎勵。但這種獨佔權是有限的。一旦到期,創新藥物就將成為後世子孫都能負擔的廉價商品。
商品化帶來的隱憂是,這很快就可能成為中國與生物製藥產業之間的社會契約——只要他們能以更低成本、更快速度生產出同等智慧財產權的產品。
但如果有一種不同的方式在生技領域建立防禦壁壘呢?
有一些早期例子指向了防禦性的正交形式。對於CAR-T 療法——一種以改造患者自身細胞來消滅癌症為核心的新型醫學形式——其通用化將呈現何種面貌尚難預料。在科爾欽斯基關於《生物技術社會契約》的書中,他實際上對此表示了擔憂。銷售這些藥物的公司可能從工藝力量而非圍繞知識產權的壟斷資源中獲得護城河。
現在讓我們隨著時間的推移向前推進。
個人化癌症疫苗是另一種具有此類形態的治療方法。這類藥物的核心並非單一的化學成分組成。相反,每一劑都是透過患者測量數據、演算法和生產步驟的複雜組合而製成。
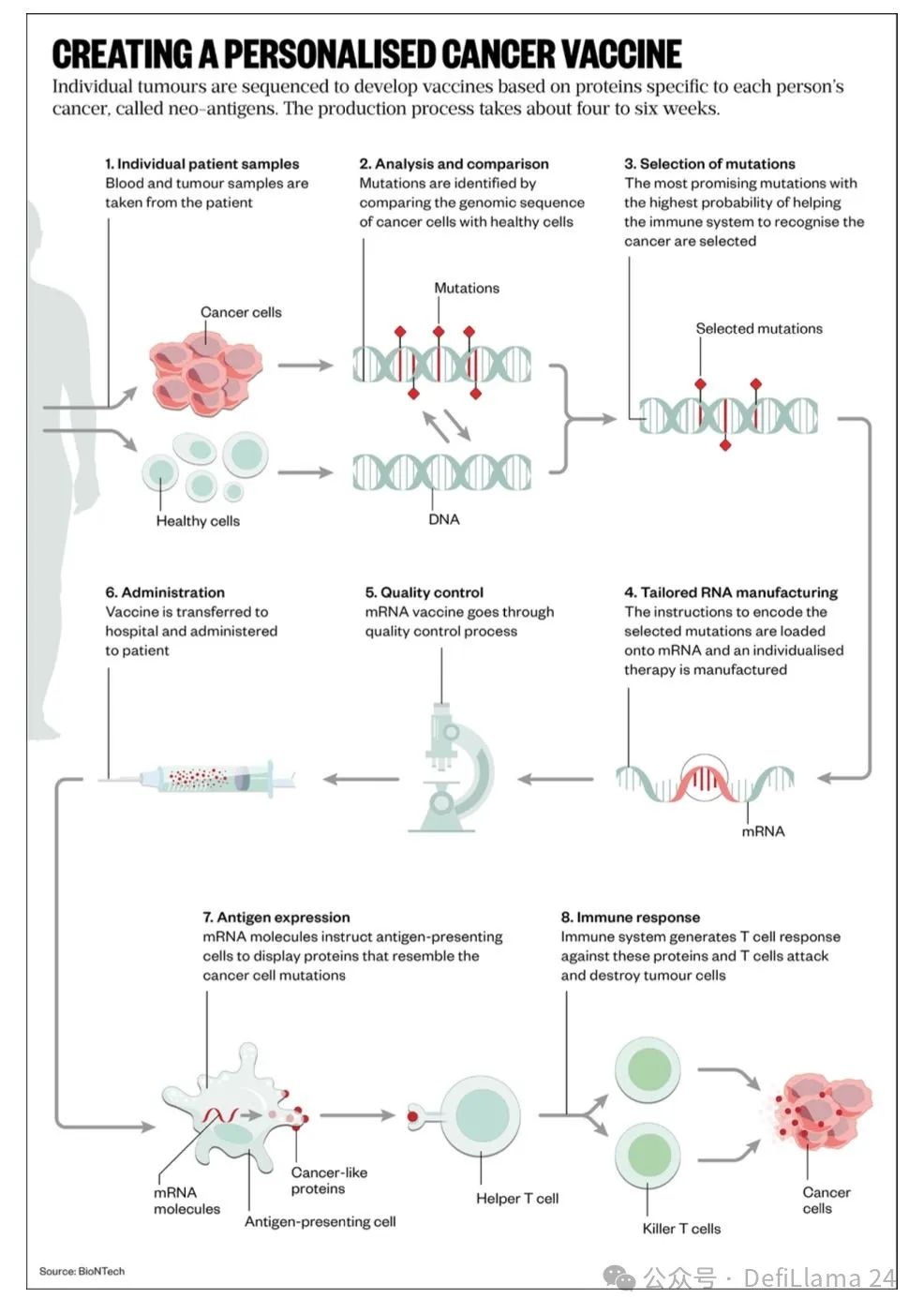
這帶來了非常有趣的後果。這可能是第一種具有網路經濟效應的藥物。由於每一劑藥物都是透過演算法設計的,隨著收集的數據增多,其品質可以提升。患者可以從擁有最大數據障礙的公司生產的藥物中獲益。這種方法顯然也受益於流程力量。隨著時間的推移,作為市場領導者,這種新模式的贏家甚至可能累積明顯的品牌優勢。
如果更多形式的藥物開始呈現這種趨勢,我們可能會看到一波生技公司直接競爭,試圖將自己確立為全新一代的製藥公司。
想到這裡,我不禁想起我的好友Packy McCormick 關於垂直整合者的論述。用他的話來說,這些公司有幾個決定性特徵:
垂直整合企業是指那些:
- 整合多項前沿且經過驗證的技術。
- 在其技術棧中發展出重要的內部能力。
- 模組化標準化組件,同時掌控整體系統整合。
- 直接與現有產業巨頭競爭。
- 提供更優質、更快速或更經濟的產品(通常三者兼具)。
對垂直整合者而言,整合本身就是創新。
和以往一樣,這項策略面臨明顯挑戰。天下沒有白吃的午餐!
一個巨大的障礙很可能是融資和資本形成。這種公司創建方式與大多數生技投資者考慮產生回報的方式完全不同。目前完全不清楚大型製藥公司是否願意在沒有明確商業可行性證明的情況下收購擁有如此複雜產品的公司。
該領域的贏家可能需要另尋資金來源。一個可行的選擇是利用日益壯大的"深度科技"風險資本池,這類資本專注於支持硬體領域的突破性進展和原子世界的創新。後期投資可能來自綜合性成長型股權公司,而非傳統的生物科技跨界基金。
在生物技術領域嘗試打造垂直整合者,絕非膽小者所能勝任。
以新方式融合多種技術實屬不易。融資將充滿挑戰。擴大商業化努力同樣艱難。成功可能需要遠比預期更長的時間。
鑑於所有這些因素,生技投資可能開始反映私募市場的整體演變趨勢。企業可能會延長私有化狀態的時間。以SpaceX 為例,這家公司在私有化的23 年間籌集了近100 億美元資金,目前估值已達3,500 億美元。早期投資者和員工的流動性主要來自二級市場,而非併購交易或首次公開發行。
儘管困難重重,潛在的回報卻是巨大的。
曾經難以想的測量工具如今在生物學領域已司空見慣。催生上一代生物科技浪潮的基礎洞見已精煉並商品化。人工智慧正在加速生物學轉向預測性和定量學科的轉變。
解決癌症、傳染病和大腦健康等以往方法難以應對的重大問題,可能需要整合多種數位與實體建構模組的創新解決方案。
如果這些解決全球問題的公司以新方式建立護城河,我們可能會見證第一批市值超過1 兆美元的生技企業誕生。
目前公開生物技術市場的情況相當黯淡。對美國生技公司而言,中國收購活動的持續升溫進一步威脅了它們的成功前景。正如Adam Feuerstein 所寫:“市場情緒糟糕透頂,悲觀氛圍揮之不去,以至於人們開始嚴肅質疑這個行業是否還有翻身的可能。”
同時,早期市場充滿潛力。科技創新的步伐同樣迅猛。那些汲取了寶貴經驗並掌握強大工具的創業家們,正在追求全新的理念。
或許正確的問題不是市場是否會反彈。因為它終將反彈。市場是周期性的。相反,問題在於生物技術是否正處於向全新階段轉變的邊緣。如果是這樣,那麼現在正是創業的最佳時機。
換句話說…
生物科技已死。生技萬歲!
免責聲明:文章中的所有內容僅代表作者的觀點,與本平台無關。用戶不應以本文作為投資決策的參考。
您也可能喜歡
前紐約州州長安德魯·科莫在聯邦調查中為OKX提供建議:彭博社
快速摘要 據彭博社報導,前紐約州州長安德魯·科莫「定期」與OKX的高管交談,並「指導他們如何應對刑事調查」。報導還稱,科莫敦促OKX邀請前紐約金融服務部主管琳達·萊斯威爾加入交易所董事會

DTCC推出用於抵押品代幣化的區塊鏈平台
簡要介紹 現代經濟的基石——存託信託與結算公司(DTCC)已經推出了一個使用Besu以太坊客戶端的代幣化實時抵押品管理平台。這個被稱為AppChain的平台旨在提高抵押品在傳統“孤立”系統之間流動的速度。

這個去中心化自治組織支付了一名英國人40萬美元製作品牌食品,現在他們在詢問他們的烘豆去哪了
簡述 前Sublime Butter執行長Chris Mair正在尋求Nouns DAO的支持,以重新啟動MOOØNBEANS烤豆項目。該項目在獲得135 ETH資金後從未啟動。Sublime董事Tony Ho告訴The Block,公司因Mair行為不穩而解僱了他,並且從未同意接受來自DAO的資金。

渣打銀行表示Avalanche的AVAX代幣價格到2029年可能飆升至250美元
快速摘要 根據渣打銀行的Geoffrey Kendrick表示,Avalanche的AVAX代幣價格到2029年底可能會上漲超過10倍。Kendrick指出,Avalanche最近的Etna升級使其對開發者來說更便宜且更具吸引力。

